مولاليته
مولاليتهي
هر جز در
محلول برابر
نسبت تعداد
مول آن جز به
جرم حلال
برحسب
كيلوگرم است.
مولاليته
بيانگر تعداد
مول حل شونده
در هر كيلوگرم
از حلال است.
واحد مولاليته
![]() يا
به طور خلاصه
يا
به طور خلاصه ![]() است كه آن را
مولال ميناميم
و با m نمايش ميدهيم.
براي
مولالیته
داريم:
است كه آن را
مولال ميناميم
و با m نمايش ميدهيم.
براي
مولالیته
داريم:
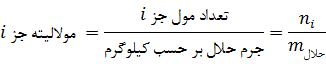
با توجه به تعریف مولالیته، تعداد مول هر جز در محلول برابر حاصلضرب مولالیته آن جز و جرم حلال بر حسب کیلوگرم است:
![]()
همچنین
برای آنکه در
یک محلول با
مولالیته مشخص
نسبت به جز i،
تعداد مول جز i
برابر ![]() باشد،
جرم حلال بایستی
باشد،
جرم حلال بایستی
![]() کیلوگرم
باشد که
کیلوگرم
باشد که ![]() از
رابطه زیر
بدست می آید:
از
رابطه زیر
بدست می آید:
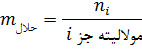
مثال: 50g اتانول ![]() آب
آب ![]() را
با هم مخلوط
كرده و محلول
يكنواختي به
دست آورده ايم.
مولاليتهي
را
با هم مخلوط
كرده و محلول
يكنواختي به
دست آورده ايم.
مولاليتهي ![]() را
در محلول حساب
كنيد.
را
در محلول حساب
كنيد.
حل:
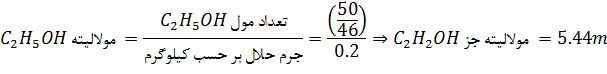
*****
مثال:
برای تهیه 1500 g محلول ![]() به
چند گرم
به
چند گرم ![]() و
چند گرم آب
نیاز داریم؟
و
چند گرم آب
نیاز داریم؟
حل:
فرض
کنیم به m
گرم ![]() نیاز
داریم.
دراینصورت
خواهیم داشت:
نیاز
داریم.
دراینصورت
خواهیم داشت:
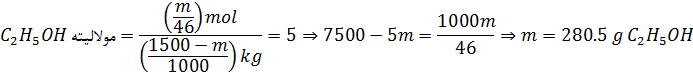
مابقی جرم محلول آب است و داریم:
![]()
*****
مثال: محلولهاي
6m و 8m از ![]() را
به چه نسبت
جرمي با هم
مخلوط كنيم تا
محلول 7m اتانول به
دست آيد؟
را
به چه نسبت
جرمي با هم
مخلوط كنيم تا
محلول 7m اتانول به
دست آيد؟
حل:
روش اول:
فرض كنيم
اگر ![]() گرم
محلول 6m را با
گرم
محلول 6m را با ![]() گرم
محلول 8m مخلوط
كنيم،
گرم
محلول 8m مخلوط
كنيم، ![]() گرم
محلول 7m خواهيم
داشت.
گرم
محلول 7m خواهيم
داشت.
در محلول 6m به ازاي هر 1000g آب ![]() گرم
اتانول داريم.
پس به ازاي هر
گرم
اتانول داريم.
پس به ازاي هر ![]() محلول،
6 مول
اتانول و 1000g آب داریم.
يعني:
محلول،
6 مول
اتانول و 1000g آب داریم.
يعني:
![]()
در محلول ![]() به
ازاي هر
به
ازاي هر ![]() آب
آب
![]() گرم اتانول
داريم. پس به
ازاي هر 1368g محلول، 1000g آب و 8 مول
اتانول داريم.
يعني:
گرم اتانول
داريم. پس به
ازاي هر 1368g محلول، 1000g آب و 8 مول
اتانول داريم.
يعني:
![]()
موقع اختلاط تعداد مول اتانول در هر محلول با هم و جرم حلالها در دو محلول با هم جمع ميشوند و براي محلول حاصله داريم:
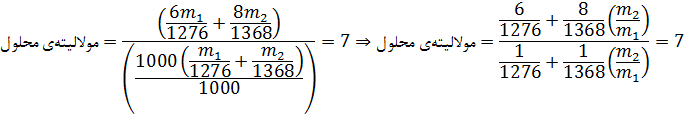
![]()
روش دوم:
فرض كنيم
از محلول 6m
مقداری برمی داريم
كه ![]() حلال
داشته باشد،
دراینصورت 6
مول هم حل
شونده خواهد
داشت. همچنين
از محلول
حلال
داشته باشد،
دراینصورت 6
مول هم حل
شونده خواهد
داشت. همچنين
از محلول ![]() مقداري
برداريم كه
مقداري
برداريم كه ![]() حلال
داشته باشيم، دراینصورت 8
مول هم حل
شونده خواهد
داشت. سپس اين
دو را با هم
مخلوط ميكنيم.
برای
مولالیته
اتانول در
محلول نهایی خواهيم
داشت:
حلال
داشته باشيم، دراینصورت 8
مول هم حل
شونده خواهد
داشت. سپس اين
دو را با هم
مخلوط ميكنيم.
برای
مولالیته
اتانول در
محلول نهایی خواهيم
داشت:
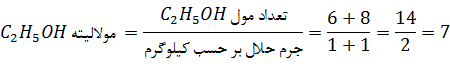
يعني محلولها بايد به نسبتي مخلوط شوند كه جرم حلال برابر داشته باشند تا مولالیته نهایی برابر 7 نتیجه دهند. دراینصورت برای نسبت جرم محلولها داریم:
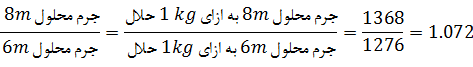
*****
||||||||||||||||||||||||||||||||||||||||||||||||||
**************************************************
سایت: www.youngchemist.com
مولف: محمد شاهی
نظرات، پیشنهادات و انتقادات: chemistry.shahi@gmail.com
**************************************************
||||||||||||||||||||||||||||||||||||||||||||||||||