محلولهاي اسيدها و بازهاي چندپروتوني ضعيف
محلول
اسید دو
ظرفیتی ضعیف
(مثل ![]() )
و مشتقاتش (مثل
)
و مشتقاتش (مثل
![]() و
و
![]() )
معمولاً در
یکی از دسته
های زیر قرار
می گیرد و
برای هر دسته
معمولاً
رابطه بیان
شده (که ساده
ترین یا
تقریبی ترین
رابطه موجود
برای آن دسته
است) صادق است:
)
معمولاً در
یکی از دسته
های زیر قرار
می گیرد و
برای هر دسته
معمولاً
رابطه بیان
شده (که ساده
ترین یا
تقریبی ترین
رابطه موجود
برای آن دسته
است) صادق است:
![]() محلول
محلول ![]() (مثلاً
محلول H2CO3 0.1 M ):
(مثلاً
محلول H2CO3 0.1 M ):
![]()
![]() محلول
محلول ![]() (مثلاً
محلول H2CO3 0.1 M
و Na+HCO3-
0.2 M):
(مثلاً
محلول H2CO3 0.1 M
و Na+HCO3-
0.2 M):
![]()
![]() محلول
محلول ![]() (مثلاً
محلول Na+HCO3- 0.3 M):
(مثلاً
محلول Na+HCO3- 0.3 M):

![]() محلول
محلول ![]() (مثلاً
محلول Na+HCO3- 0.2 M وM Na2CO3
0.05):
(مثلاً
محلول Na+HCO3- 0.2 M وM Na2CO3
0.05):
![]()
![]() محلول
محلول ![]() (مثلاً محلول M Na2CO3 0.15):
(مثلاً محلول M Na2CO3 0.15):
![]()
دقت
داشته باشید
که محلول حاوی
![]() جزء دسته
های ذکر شده
قرار ندارد.
این بدان علت
است که «دو
گونه با
اختلاف تعداد
پروتون برابر
جزء دسته
های ذکر شده
قرار ندارد.
این بدان علت
است که «دو
گونه با
اختلاف تعداد
پروتون برابر ![]() یا
بیشتر
معمولاً با هم
واکنش کمی می
دهند و به
گونه هایی که
اختلاف تعداد
پروتون آنها
کمتر از
یا
بیشتر
معمولاً با هم
واکنش کمی می
دهند و به
گونه هایی که
اختلاف تعداد
پروتون آنها
کمتر از ![]() است
تبدیل می
شوند». واکنشهای
زیر را می
توان به عنوان
مثال برای قاعده
بالا در نظر
گرفت:
است
تبدیل می
شوند». واکنشهای
زیر را می
توان به عنوان
مثال برای قاعده
بالا در نظر
گرفت:
![]()
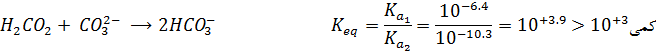

![]()
![]()
در مورد ![]() و
و ![]() واکنش
بصورت زیر
خواهد بود:
واکنش
بصورت زیر
خواهد بود:
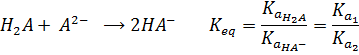
از
آنجائیکه
معمولاً ![]() است،
است،
![]() معمولاً
بزرگتر از
معمولاً
بزرگتر از ![]() خواهد
بود و واکنش
بالا می تواند
معمولاً کمی
فرض شود.
بنابراین
محلول
خواهد
بود و واکنش
بالا می تواند
معمولاً کمی
فرض شود.
بنابراین
محلول ![]() و
و ![]() به یکی
از سه صورت:
محلول
به یکی
از سه صورت:
محلول ![]() و
و ![]() (در
صورت اضافه
بودن
(در
صورت اضافه
بودن ![]() )،
محلول
)،
محلول ![]() و
و ![]() (در صورت
اضافه بودن
(در صورت
اضافه بودن ![]() )
و محلول
)
و محلول ![]() (در صورت
مساوی بودن
(در صورت
مساوی بودن ![]() و
و ![]() )
تبدیل خواهد
شد.
)
تبدیل خواهد
شد.
در مورد
محلول ![]() بایستی
بخاطر سپرد که
معمولاً می
توان از
بایستی
بخاطر سپرد که
معمولاً می
توان از ![]() ناشی
از تفکیک دوم
صرف نظر نمود.
این بدان علت
است که ثابت
تعادل واکنش
دوم معمولاً
بسیار کوچکتر
از ثابت تعادل
واکنش اول است
(
ناشی
از تفکیک دوم
صرف نظر نمود.
این بدان علت
است که ثابت
تعادل واکنش
دوم معمولاً
بسیار کوچکتر
از ثابت تعادل
واکنش اول است
(![]() )
و همچنین ماده
اولیه واکنش
دوم یعنی
)
و همچنین ماده
اولیه واکنش
دوم یعنی ![]() از
واکنش تفکیک
اول که
معمولاً به
مقدار ناچیزی
پیشرفت می کند
و غیرکمی است،
حاصل می شود (
از
واکنش تفکیک
اول که
معمولاً به
مقدار ناچیزی
پیشرفت می کند
و غیرکمی است،
حاصل می شود (![]() ).
تحت این شرایط
مسئله محاسبه
).
تحت این شرایط
مسئله محاسبه ![]() محلول
محلول ![]() مشابه
مسئله محاسبه
مشابه
مسئله محاسبه ![]() محلول
یک اسید ضعیف
تک پروتونی با
همان غلظت و
محلول
یک اسید ضعیف
تک پروتونی با
همان غلظت و ![]() است
که در ساده
ترین حالت رابطه
است
که در ساده
ترین حالت رابطه
![]() را
نتیجه می دهد.
مشابه همین
بحث را می
توان برای
محلول حاوی
تنها یک باز
دو پروتونی
ضعیف ارائه
نمود و در
ساده ترین
حالت رابطه
را
نتیجه می دهد.
مشابه همین
بحث را می
توان برای
محلول حاوی
تنها یک باز
دو پروتونی
ضعیف ارائه
نمود و در
ساده ترین
حالت رابطه ![]() را
برای آن نتیجه
گرفت.
را
برای آن نتیجه
گرفت.
در مورد
محلولهای ![]() یا
یا ![]() معمولاً
می توان از
حضور گونه سوم
(مثلاً
معمولاً
می توان از
حضور گونه سوم
(مثلاً ![]() در مورد
اول یا
در مورد
اول یا ![]() در مورد
دوم) چشم
پوشید و مسئله
را مشابه مسئله
محلول حاوی یک
اسید و باز
مزدوج ضعیف تک
پروتونی در
حضور هم فرض
کرد که در
ساده ترین
حالت،
در مورد
دوم) چشم
پوشید و مسئله
را مشابه مسئله
محلول حاوی یک
اسید و باز
مزدوج ضعیف تک
پروتونی در
حضور هم فرض
کرد که در
ساده ترین
حالت، ![]() محلول را از
رابطه
هندرسون – هسل
باخ بر مبنای
محلول را از
رابطه
هندرسون – هسل
باخ بر مبنای ![]() فرم
اسیدی حاضر در
محلول (
فرم
اسیدی حاضر در
محلول (![]() در
مورد اول و
در
مورد اول و ![]() در
مورد دوم )
بدست می
آوریم.
در
مورد دوم )
بدست می
آوریم.
مشابه
بحث بافر برای
زوج اسید و
باز ضعیف مزدوج،
زوجهای ![]() و
و
![]() نیز
می توانند در
صورت بالا
بودن غلظت های
اسید و باز
مزدوج و نزدیک
بودن نسبت
غلظت ها به 1 خصلت
بافری از خود
نشان دهند.
زوج
نیز
می توانند در
صورت بالا
بودن غلظت های
اسید و باز
مزدوج و نزدیک
بودن نسبت
غلظت ها به 1 خصلت
بافری از خود
نشان دهند.
زوج ![]() می
تواند برای
تثبیت
می
تواند برای
تثبیت ![]() در نزدیکی
در نزدیکی ![]() و
زوج
و
زوج ![]() می
تواند برای
تثبیت
می
تواند برای
تثبیت ![]() در نزدیکی
در نزدیکی ![]() بکار
رود.
بکار
رود.
مثال: می خواهیم
با اضافه کردن
![]() به
محلول
به
محلول ![]() ،
بافر بدست
بیاوریم. چند
مول سود
بایستی به هر
لیتر محلول
اسیدکربنیک
یک مولار
اضافه کنیم تا
بافری با
،
بافر بدست
بیاوریم. چند
مول سود
بایستی به هر
لیتر محلول
اسیدکربنیک
یک مولار
اضافه کنیم تا
بافری با ![]() برابر:
برابر:
الف ) ![]() ب )
ب ) ![]() بدست آوریم؟
از تغییر حجم
موقع اختلاط
صرف نظر کنید.
بدست آوریم؟
از تغییر حجم
موقع اختلاط
صرف نظر کنید.
![]()
حل:
الف) از
آنجائیکه ![]() داده
شده در محدوده
داده
شده در محدوده
![]() و
و ![]() قرار
دارد، می توان
از زوج
قرار
دارد، می توان
از زوج ![]() برای
تهیه بافر
مربوطه
استفاده نمود.
مقدار مول سود
اضافه شده
بایستی به
گونه ای تنظیم
شود که نسبت
غلظت های
برای
تهیه بافر
مربوطه
استفاده نمود.
مقدار مول سود
اضافه شده
بایستی به
گونه ای تنظیم
شود که نسبت
غلظت های ![]() باقیمانده
و
باقیمانده
و ![]() تولید
شده
تولید
شده ![]() مطلوب
را نتیجه دهد.
برای تعیین
مقدار مول سود
مورد نیاز به
صورت زیر عمل
می کنیم:
مطلوب
را نتیجه دهد.
برای تعیین
مقدار مول سود
مورد نیاز به
صورت زیر عمل
می کنیم:

![]()
![]()

![]()
بنابراین
در صورتی که
به هر لیتر
محلول اسید کربنیک
یک مولار، ![]() سود
سوزآور اضافه
کنیم، یک لیتر
محلول
سود
سوزآور اضافه
کنیم، یک لیتر
محلول ![]() و
و![]() با
با ![]() برابر
برابر
![]() بدست می
آوریم که چون
غلظت های
بدست می
آوریم که چون
غلظت های ![]() و
و ![]() نسبتاً
قابل توجه و
نسبت آنها بین
نسبتاً
قابل توجه و
نسبت آنها بین
![]() و
و
![]() است،
برای محلول
حاصل می توان
خصلت بافری در
نظر گرفت.
است،
برای محلول
حاصل می توان
خصلت بافری در
نظر گرفت.
ب) از
آنجائیکه ![]() داده
شده در محدوده
داده
شده در محدوده
![]() و
و ![]() قرار
دارد، می توان
از زوج
قرار
دارد، می توان
از زوج ![]() برای
تهیه بافر
مربوطه
استفاده نمود.
برای تعیین
مقدار مول سود
موردنیاز به
صورت زیر عمل
می کنیم:
برای
تهیه بافر
مربوطه
استفاده نمود.
برای تعیین
مقدار مول سود
موردنیاز به
صورت زیر عمل
می کنیم:

![]()
![]()

![]()
![]()
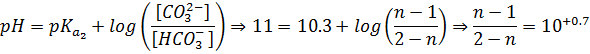
![]()
بنابراین
در صورتی که ![]() مول
سود سوزآور به
هر لیتر محلول
اسیدکربنیک یک
مولار اضافه
کنیم، یک لیتر
محلول
مول
سود سوزآور به
هر لیتر محلول
اسیدکربنیک یک
مولار اضافه
کنیم، یک لیتر
محلول ![]() و
و ![]() با
با ![]() برابر
برابر ![]() و
خصلت بافری
بدست می
آوریم.
و
خصلت بافری
بدست می
آوریم.
*****
مشابه
بحث محلول
حاوی اسید دو
ظرفیتی و
مشتقاتش،
محلول حاوی
اسید سه
ظرفیتی ضعیف
(مثل ![]() )
و مشتقاتش نیز
معمولاً در
یکی از دسته
های زیر با
رابطه داده
شده برای
محاسبه
)
و مشتقاتش نیز
معمولاً در
یکی از دسته
های زیر با
رابطه داده
شده برای
محاسبه ![]() قرار
می گیرد.
قرار
می گیرد.
![]() محلول
محلول ![]() (مثلاً
محلول
(مثلاً
محلول ![]() )
)
![]()
![]() محلول
محلول ![]() و
و ![]() (مثلاً
محلول
(مثلاً
محلول ![]() و
و ![]() )
)
![]()
![]() محلول
محلول ![]() (مثلاً
محلول
(مثلاً
محلول ![]() )
)

![]() محلول
محلول![]() و
و![]() (مثلاً
محلول
(مثلاً
محلول ![]() و
و ![]() )
)
![]()
![]() محلول
محلول ![]() (مثلاً
محلول
(مثلاً
محلول ![]() )
)

![]() محلول
محلول ![]() و
و
![]() (مثلاً
محلول
(مثلاً
محلول ![]() و
و ![]() )
)
![]()
![]() محلول
محلول ![]() (مثلاً
محلول
(مثلاً
محلول ![]() )
)
![]()
مشابه
حالت
دوپروتونی،
زوجهای ![]() ،
،
![]() و
و ![]() در
صورت دارا
بودن شرایط
مربوط به بافر
یعنی نسبت
غلظت اسید و
باز مزدوج بین
در
صورت دارا
بودن شرایط
مربوط به بافر
یعنی نسبت
غلظت اسید و
باز مزدوج بین
![]() و
و ![]() و بالا بودن
غلظت های اسید
و باز مزدوج
دارای خصلت
بافری خواهند
بود و می
توانند به
ترتیب برای
تثبیت
و بالا بودن
غلظت های اسید
و باز مزدوج
دارای خصلت
بافری خواهند
بود و می
توانند به
ترتیب برای
تثبیت ![]() در
نزدیکی
در
نزدیکی ![]() ،
،
![]() و
و
![]() بکار
روند.
بکار
روند.
برای حالت چهار پروتونی و بیشتر نیز می توان بطور کاملاً مشابه بحث نمود و روابط مربوطه را بدست آورد.
مثال: ![]() هریک از
محلولهای زیر
را بدست
آورید.
هریک از
محلولهای زیر
را بدست
آورید.
الف) ![]()
ب) ![]() و
و
![]()
ج) ![]()
د) ![]() و
و ![]()
ه) ![]()
و) ![]()
ز) ![]() ،
،
![]() و
و ![]()
ح) ![]() و
و ![]()
![]()
حل:
الف)

ب) زوج ![]() در
حضور هم داریم
که برای آن می
نویسیم:
در
حضور هم داریم
که برای آن می
نویسیم:
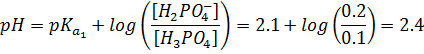
ج ) برای
آمفوتر ![]() داریم:
داریم:
![]()
د) ساده
ترین رابطه
برای محاسبه ![]() این محلول
به صورت زیر
خواهد بود:
این محلول
به صورت زیر
خواهد بود:

ه) برای
محاسبه ![]() این
محلول به صورت
زیر عمل می
کنیم:
این
محلول به صورت
زیر عمل می
کنیم:
![]()
و)

ز) ابتدا
بایستی واکنش
کمی ![]() با
با ![]() را
در نظر بگیریم:
را
در نظر بگیریم:

![]()
![]()
محلول
نهایی شامل ![]() و
و
![]() است
که برای
محاسبه
است
که برای
محاسبه ![]() آن
داریم:
آن
داریم:

ح) ابتدا بایستی واکنش کمی زیر را در نظر بگیریم:

![]()
![]()
محلول در
اثر واکنش
یادشده به
صورت محلول ![]() ،
،
![]() و
و
![]() در
خواهد آمد که
برای آن
بایستی واکنش
کمی زیر را
نظر بگیریم:
در
خواهد آمد که
برای آن
بایستی واکنش
کمی زیر را
نظر بگیریم:

![]()
![]()
محلول
نهایی شامل ![]() و
و
![]() خواهد
بود که برای
محاسبه
خواهد
بود که برای
محاسبه ![]() آن
داریم:
آن
داریم:
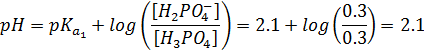
*****
مثال: می
خواهیم با
اضافه کردن و
حل کردن سدیم
فسفات در
محلول اسید
فسفریک ![]() مولار،
بافر با
مولار،
بافر با ![]() تثبیت
شده در
تثبیت
شده در ![]() بدست
آوریم. به هر
لیتر محلول
اسید فسفریک
بدست
آوریم. به هر
لیتر محلول
اسید فسفریک ![]() مولار
بایستی
چندگرم نمک سدیم
فسفات اضافه
کنیم؟ اختلاط
را بدون تغییر
حجم فرض کنید.
در صورتیکه به
هر لیتر بافر
تهیه شده
مولار
بایستی
چندگرم نمک سدیم
فسفات اضافه
کنیم؟ اختلاط
را بدون تغییر
حجم فرض کنید.
در صورتیکه به
هر لیتر بافر
تهیه شده ![]() مول
اسید
کلریدریک
مول
اسید
کلریدریک ![]() اضافه
کنیم، مقدار
تغییر
اضافه
کنیم، مقدار
تغییر ![]() چقدر
خواهد بود؟
چقدر
خواهد بود؟
![]()
حل:
با توجه
به اینکه ![]() مدنظر
برای بافر در
نزدیکی
مدنظر
برای بافر در
نزدیکی ![]() قرار
دارد، بافر
شامل زوج
قرار
دارد، بافر
شامل زوج ![]() خواهد
بود که نسبت
غلظت آنها
بصورت زیر
محاسبه می شود:
خواهد
بود که نسبت
غلظت آنها
بصورت زیر
محاسبه می شود:

![]() و
و
![]() با این نسبت
غلظت ها را
بایستی از
واکنش
با این نسبت
غلظت ها را
بایستی از
واکنش ![]() با
با
![]() بدست
آوریم. مقدار
گرم مورد نیاز
سدیم فسفات برای
هر لیتر محلول
اسیدفسفریک
را
بدست
آوریم. مقدار
گرم مورد نیاز
سدیم فسفات برای
هر لیتر محلول
اسیدفسفریک
را ![]() در
نظر می گیریم.
برای محاسبه
در
نظر می گیریم.
برای محاسبه ![]() به شیوه
های مختلفی می
توانیم عمل
کنیم.
به شیوه
های مختلفی می
توانیم عمل
کنیم.
یک شیوه
می تواند
براین اساس
باشد که ![]() های
موجود در
های
موجود در ![]() و
و
![]() از
از
![]() های
موجود در
های
موجود در ![]() اولیه
نشأت گرفته
اند و بایستی
داشته باشیم:
اولیه
نشأت گرفته
اند و بایستی
داشته باشیم:
![]()
رابطه بالا در ترکیب با نسبت غلظت های بدست آمده نتیجه می دهد که :
![]()
مقدار ![]() با درنظر
گرفتن موازنه
جرم برای گونه
فسفات و
مشتقاتش به
صورت زیر
محاسبه می شود:
با درنظر
گرفتن موازنه
جرم برای گونه
فسفات و
مشتقاتش به
صورت زیر
محاسبه می شود:
![]()
![]()
یک شیوه
دیگر می تواند
براین اساس
باشد که واکنش
![]() با
با
![]() با
مقادیر مولی
برابر ،
با
مقادیر مولی
برابر ، ![]() و
و
![]() با
مقادیر مولی
برابر می دهد،
در حالیکه
برای بافر
موردنیاز،
غلظت و تعداد
مول
با
مقادیر مولی
برابر می دهد،
در حالیکه
برای بافر
موردنیاز،
غلظت و تعداد
مول ![]() کمتر
از
کمتر
از ![]() است.
بنابراین در
واکنش
است.
بنابراین در
واکنش ![]() با
با
![]() ،
،
![]() بایستی
محدود کننده
باشد تا مقدار
اضافی
بایستی
محدود کننده
باشد تا مقدار
اضافی ![]() با مقداری از
با مقداری از ![]() تولید
شده واکنش دهد
و منجر به
کاهش غلظت
تولید
شده واکنش دهد
و منجر به
کاهش غلظت ![]() و
افزایش غلظت
و
افزایش غلظت ![]() شود
و در نهایت
نسبت غلظت
مورد نیاز را
بدست دهد. در
این صورت برای
بدست آوردن
شود
و در نهایت
نسبت غلظت
مورد نیاز را
بدست دهد. در
این صورت برای
بدست آوردن ![]() به صورت
زیر عمل می
کنیم:
به صورت
زیر عمل می
کنیم:
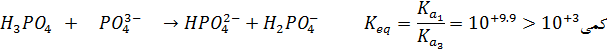
![]()
![]()

![]()

![]()

برای
بافر غلظت ![]() و
و
![]() بصورت
زیر خواهد بود:
بصورت
زیر خواهد بود:
![]()
برای
محاسبه تغییر ![]() براثر
اضافه کردن
براثر
اضافه کردن ![]() مول
مول
![]() به
هر لیتر بافر
می توانیم به
صورت زیر عمل
کنیم:
به
هر لیتر بافر
می توانیم به
صورت زیر عمل
کنیم:
واکنش
کمی ![]() با
با
![]() اضافه
شده را بصورت
زیر درنظر می
گیریم:
اضافه
شده را بصورت
زیر درنظر می
گیریم:

![]()
![]()
محلول
نهایی شامل ![]() و
و
![]() خواهد
بود که برای
محاسبه
خواهد
بود که برای
محاسبه ![]() آن
داریم:
آن
داریم:

![]()
*****
||||||||||||||||||||||||||||||||||||||||||||||||||
**************************************************
سایت: www.youngchemist.com
مولف: محمد شاهی
نظرات، پیشنهادات و انتقادات: chemistry.shahi@gmail.com
**************************************************
||||||||||||||||||||||||||||||||||||||||||||||||||